Ιατρικός εμπειρογνώμονας του άρθρου
Νέες δημοσιεύσεις
Επαναστένωση
Τελευταία επισκόπηση: 04.07.2025

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.
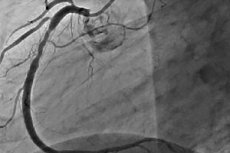
Η επαναστένωση είναι η ανάπτυξη υποτροπιάζουσας στένωσης 50% ή περισσότερο στο σημείο της διαδερμικής στεφανιαίας επέμβασης. Η επαναστένωση συνήθως συνοδεύεται από υποτροπιάζουσα στηθάγχη, η οποία συχνά απαιτεί επαναλαμβανόμενες παρεμβάσεις. Καθώς η PCI έχει εξελιχθεί, η συχνότητα εμφάνισης της επαναστένωσης έχει μειωθεί και η φύση της έχει επίσης αλλάξει.
Επαναστένωση μετά από αγγειοπλαστική στεφανιαίων αγγείων με διαυλικό μπαλόνι (TBCA)
Μετά από TBCA, το ποσοστό επαναστένωσης τους πρώτους 6 μήνες είναι 30-40%. Ο κύριος μηχανισμός ανάπτυξής της είναι η τοπική αρνητική αναδιαμόρφωση του αγγείου, η οποία, ουσιαστικά, είναι μια ελαστική κατάρρευση του αρτηριακού αυλού, που διαστέλλεται από το μπαλόνι κατά τη διάρκεια της επέμβασης. Ο τοπικός σχηματισμός θρόμβου και η ανάπτυξη του νεοενδοθηλίου παίζουν επίσης σχετικό ρόλο. Υπάρχουν κλινικοί (σακχαρώδης διαβήτης τύπου 2, οξύ στεφανιαίο σύνδρομο (ACS), ιστορικό επαναστένωσης), αγγειογραφικοί (βλάβη LAD, μικρή διάμετρος αγγείου, χρόνια ολική απόφραξη (CTO), μακρά βλάβη, εκφυλισμένα μοσχεύματα φλεβικής παράκαμψης) και διαδικαστικοί (μεγάλη υπολειμματική στένωση, μικρή αύξηση της διαμέτρου του αγγείου ως αποτέλεσμα του φουσκώματος του μπαλονιού) παράγοντες κινδύνου για επαναστένωση μετά από TBCA. Σε περίπτωση επαναστένωσης, συνήθως πραγματοποιείται επαναλαμβανόμενη παρέμβαση. Η επιτυχία της επαναλαμβανόμενης TBCA στο σημείο της επαναστένωσης είναι συγκρίσιμη με την πρώτη επέμβαση. Ωστόσο, με κάθε επόμενη TBCA για επαναστένωση, ο κίνδυνος υποτροπιάζουσας επαναστένωσης αυξάνεται σημαντικά. Μετά την 3η προσπάθεια, φτάνει το 50-53%. Επιπλέον, με κάθε επαναλαμβανόμενη TBCA, η αναπτυσσόμενη επαναστένωση είναι πιο έντονη από την πρώτη. Παράγοντες κινδύνου για επαναστένωση μετά τη δεύτερη TBCA είναι η πρώιμη εμφάνιση της πρώτης επαναστένωσης (60-90 ημέρες μετά τη διαδικασία), η βλάβη του LAD, η πολυαγγειακή βλάβη, ο σακχαρώδης διαβήτης τύπου 2, η αρτηριακή υπέρταση, η ασταθής στηθάγχη και οι πολλαπλές διογκώσεις μπαλονιών κατά τη διάρκεια της πρώτης διαδικασίας. Δεδομένης της υψηλής συχνότητας επαναστένωσης και του μηχανισμού ανάπτυξής της, εισήχθησαν στην κλινική πράξη τα στεφανιαία στεντ, τα οποία θεωρητικά θα έπρεπε να είχαν εξαλείψει την αρνητική αναδιαμόρφωση των αγγείων μετά από TBCA.
Οι πρώτες μελέτες που απέδειξαν την αποτελεσματικότητα της τοποθέτησης stent ήταν οι μελέτες STRESS και BENESTENT, οι οποίες δημοσιεύθηκαν το 1993. Η BENESTENT περιελάμβανε 516 ασθενείς με νεοδιαγνωσμένη στένωση σε στεφανιαίες αρτηρίες με διάμετρο μεγαλύτερη από 3 mm, οι οποίοι τυχαιοποιήθηκαν σε δύο ομάδες: συμβατική TBCA (n = 257) και TBCA με τοποθέτηση stent (n = 259). Μετά από 3 χρόνια, το ποσοστό επαναστένωσης κατά τη διάρκεια της αγγειογραφίας ήταν 32% στην ομάδα συμβατικής TBCA και 22% στην ομάδα τοποθέτησης stent. Η σχετική μείωση του ποσοστού επαναστένωσης ήταν 31% (p < 0,01). Η ομάδα τοποθέτησης stent είχε επίσης χαμηλότερη ανάγκη για επαναλαμβανόμενη μυοκαρδιακή επαναγγείωση (10% έναντι 20,6% στην ομάδα συμβατικής TBCA, p < 0,01), η οποία συσχετίστηκε με χαμηλότερο ποσοστό υποτροπής στηθάγχης στην ομάδα τοποθέτησης stent.
Σύμφωνα με τη μελέτη STRESS (n = 407), το ποσοστό επαναστένωσης ήταν επίσης χαμηλότερο στην ομάδα τοποθέτησης stent (n ~ 205) σε σχέση με την ομάδα συμβατικής PTCA (n = 202) - 31,6 έναντι 42,1% (p < 0,01). Το πλεονέκτημα της χρήσης stent έναντι της συμβατικής αγγειοπλαστικής σε περίπτωση επαναστένωσης στη θέση PTCA αποδείχθηκε στη μελέτη REST, στην οποία 383 ασθενείς με επαναστένωση τυχαιοποιήθηκαν σε τοποθέτηση stent ή επαναλαμβανόμενη διαδερμική διαυλική αγγειοπλαστική στεφανιαίων. Η αγγειογραφικά ανιχνευμένη επαναλαμβανόμενη επαναστένωση ήταν 18% χαμηλότερη στην ομάδα τοποθέτησης stent (18 έναντι 5,32%, p < 0,03). Η επαναλαμβανόμενη μυοκαρδιακή επαναγγείωση, η οποία αποτελεί δείκτη κλινικά σημαντικής επαναστένωσης, απαιτήθηκε επίσης σημαντικά λιγότερο συχνά στην ομάδα των ασθενών που υποβλήθηκαν σε τοποθέτηση stent (10 έναντι 27%, p < 0,001). Έτσι, καλύτερα αποτελέσματα με τη χρήση stent αποδείχθηκαν όχι μόνο στις αυτοφυείς αρτηρίες, αλλά και στην περίπτωση παρέμβασης για επαναστένωση που αναπτύχθηκε μετά από TBCA.
Επαναστένωση μετά από εμφύτευση γυμνού stent (BSI)
Παρόλο που τα ακάλυπτα στεφανιαία στεντ έχουν μειώσει τη συχνότητα εμφάνισης επαναστένωσης κατά 30-40% σε σύγκριση με την TBCA, το 17-32% των ασθενών αναπτύσσουν επαναστένωση εντός του στεντ ακόμη και μετά την τοποθέτηση στεντ, απαιτώντας επαναλαμβανόμενη επαναγγείωση. Ο μηχανισμός ανάπτυξης στένωσης εντός του στεντ (ISS) διαφέρει από αυτόν στην TBCA. Μετά την τοποθέτηση στεντ, η κύρια συμβολή στην επαναστένωση είναι ο σχηματισμός νεοέσω χιτώνα, και όχι η αρνητική αναδιαμόρφωση, όπως στην TBCA, η οποία ουσιαστικά απουσιάζει από τη θέση εμφύτευσης του στεντ. Ο νεοέσω χιτώνας σχηματίζεται από τη μετανάστευση και τον πολλαπλασιασμό των λείων μυϊκών κυττάρων που παράγουν εξωκυττάρια μήτρα, η οποία μαζί με τα κύτταρα αποτελεί τον νεοέσω χιτώνα. Επιπλέον, η επιμονή του θρόμβου στη θέση τοποθέτησης του στεντ είναι επίσης σημαντική σε ασθενείς με διαβήτη.
Η κύρια ταξινόμηση της στένωσης εντός του stent (ISS) είναι η ταξινόμηση που προτάθηκε από τον Mehrаn, η οποία περιλαμβάνει τέσσερις τύπους ανάλογα με την έκταση και τη σοβαρότητα της βλάβης: ISS τύπου I - τοπική (< 10 mm σε μήκος), II τύπος - διάχυτη (> 10 mm σε μήκος), III τύπος - πολλαπλασιαστική (> 10 mm και εκτείνεται πέρα από το stent) και IV τύπος - ISS που οδηγεί σε απόφραξη. Ο πρώτος τύπος διαιρείται σε υποτύπους ανάλογα με τη θέση στο stent: 1a - στην καμπή ή μεταξύ των stent, 1b - οριακή, 1c - μέσα στο stent, 1d - πολυεστιακή.
Παράγοντες κινδύνου για την ανάπτυξη VRS είναι οι επεμβάσεις σε φλεβικά μοσχεύματα bypass, οι χρόνιες αποφράξεις, οι βλάβες στα στόμια, η μικρή διάμετρος αγγείου, η παρουσία υπολειμματικής στένωσης, η τοποθέτηση stent για VRS, η μικρή μετεγχειρητική διάμετρος αγγείου, η βλάβη LAD, το μεγάλο μήκος stent, η παρουσία διαβήτη, η εμφύτευση πολλών stent σε μία βλάβη. Υπάρχουν ενδείξεις επίδρασης γενετικών παραγόντων, ιδίως ο πολυμορφισμός του γονιδίου της γλυκοπρωτεΐνης IIIa και οι μεταλλάξεις του γονιδίου της μεθυλενοτετραϋδροφυλλικής αναγωγάσης - του γονιδίου που κωδικοποιεί την ιντερλευκίνη-1. Στην περίπτωση ανάπτυξης οριακής επαναστένωσης του stent, ο κύριος παράγοντας κινδύνου είναι μια έντονη αθηροσκληρωτική βλάβη στο τμήμα που έχει τοποθετηθεί stent.
Η επαναστένωση εμφανίζεται κυρίως κατά τους πρώτους 6-8 μήνες μετά τη διαδερμική στεφανιαία επέμβαση. Οι περισσότεροι ασθενείς εμφανίζουν κλινικά συμπτώματα περίπου την ίδια χρονική περίοδο. Η VRS συνήθως εκδηλώνεται με υποτροπιάζουσα στηθάγχη. Η ασταθής στηθάγχη εμφανίζεται λιγότερο συχνά (11-41% των περιπτώσεων). Το ΟΕΜ αναπτύσσεται στο 1-6% των ασθενών. Έτσι, η πιο συχνή αιτία στηθάγχης κατά την περίοδο 1-6 μηνών μετά την τοποθέτηση stent είναι η ανάπτυξη VRS, η οποία, κατά κανόνα, απαιτεί επαναλαμβανόμενη επαναγγείωση. Υπάρχουν διάφορες μέθοδοι για τη θεραπεία της VRS. Μπορεί να πραγματοποιηθεί συμβατική TBCA, η οποία οδηγεί σε περαιτέρω διαστολή του stent (56% συμβολή στην τελική αύξηση της διαμέτρου του αγγείου) και ωθεί τον νεοέσω χιτώνα μέσω των κυττάρων του stent (44% συμβολή στην τελική αύξηση της διαμέτρου). Ωστόσο, παρατηρείται υπολειμματική επαναστένωση στις περισσότερες περιπτώσεις στο σημείο της επέμβασης (κατά μέσο όρο 18%). Επιπλέον, μετά από TBCA, απαιτείται επαναλαμβανόμενη επαναγγείωση στο 11% των περιπτώσεων, συχνότερα σε ασθενείς με πολυαγγειακή νόσο, χαμηλό LVEF, σε περίπτωση επεμβάσεων σε φλεβικά μοσχεύματα bypass ή πρώιμης εμφάνισης του πρώτου VRS. Ο κίνδυνος εμφάνισης επαναλαμβανόμενων VRS μετά από TBCA εξαρτάται επίσης από τον τύπο της βλάβης και κυμαίνεται από 10% σε περίπτωση τοπικής επαναστένωσης έως 80% σε περίπτωση απόφραξης εντός του stent. Η εμφύτευση του LES στη θέση του VRS δεν μειώνει τον κίνδυνο υποτροπής του σε σύγκριση με την TBCA μόνο.
Η δεύτερη μέθοδος αντιμετώπισης του VRS είναι η βραχυθεραπεία, η οποία περιλαμβάνει την εισαγωγή μιας ραδιενεργού πηγής στον αυλό της στεφανιαίας αρτηρίας, αποτρέποντας τον πολλαπλασιασμό των λείων μυϊκών κυττάρων και, κατά συνέπεια, μειώνοντας τον κίνδυνο επαναστένωσης. Ωστόσο, το υψηλό κόστος του εξοπλισμού, η τεχνική πολυπλοκότητα της διαδικασίας και η αυξημένη συχνότητα εμφάνισης όψιμης θρόμβωσης του στεντ (LT) έχουν αποκλείσει σχεδόν πλήρως τη βραχυθεραπεία από την κλινική χρήση.
Μια επαναστατική στιγμή στη θεραπεία του VRS ήταν η εισαγωγή stent που εκλούουν φάρμακο. Σε σύγκριση με τους LES σε φυσικές αρτηρίες, μειώνουν τον κίνδυνο VRS κατά 70-80%. Τα πρώτα δεδομένα σχετικά με την αποτελεσματικότητα του DES σε ασθενείς με ήδη ανεπτυγμένο VRS ελήφθησαν στο μητρώο ασθενών TAXUS III, στο οποίο, κατά τη χρήση SPG1 σε αυτούς τους ασθενείς, η συχνότητα υποτροπής του VRS ήταν μόνο 16% μετά από 6 μήνες, η οποία είναι χαμηλότερη από ό,τι στις προαναφερθείσες μελέτες με TBCA. Στο μητρώο TRUE, το οποίο περιελάμβανε ασθενείς μετά από εμφύτευση SES για επαναστένωση του LES, μετά από 9 μήνες, απαιτήθηκε επαναλαμβανόμενη επαναγγείωση σε λιγότερο από 5% των ασθενών, κυρίως με σακχαρώδη διαβήτη και ACS. Η μελέτη TROPICAL συνέκρινε τη συχνότητα επαναλαμβανόμενης επαναστένωσης σε ασθενείς μετά από εμφύτευση DES στο σημείο της επαναστένωσης με τα δεδομένα των μελετών GAMMA I και GAMMA II, στις οποίες χρησιμοποιήθηκε βραχυθεραπεία ως μέθοδος θεραπείας. Μετά από 6 μήνες, η συχνότητα εμφάνισης υποτροπιάζουσας επαναστένωσης ήταν σημαντικά χαμηλότερη στην ομάδα SPS (9,7 έναντι 40,3%, p < 0,0001). Είναι σημαντικό να σημειωθεί ότι η συχνότητα εμφάνισης θρόμβωσης του stent και εμφράγματος του μυοκαρδίου ήταν επίσης χαμηλότερη στην ομάδα SPS (TS 0,6 έναντι 3,9%, p = 0,08, MI - 1,8 έναντι 9,4%, p = 0,004). Το πλεονέκτημα του SPS έναντι της βραχυθεραπείας επιβεβαιώθηκε στην τυχαιοποιημένη μελέτη SISR, στην οποία 384 ασθενείς με ανεπτυγμένο VRS στο NSC τυχαιοποιήθηκαν σε ομάδες βραχυθεραπείας ή εμφύτευσης SPS. Μετά από 9 μήνες, η ανάγκη για επαναλαμβανόμενη επαναγγείωση ήταν υψηλότερη μετά από βραχυθεραπεία (19,2%) από ό,τι στην ομάδα εμφύτευσης SPS (8,5%), γεγονός που αντανακλούσε μια πιο συχνή υποτροπή της επαναστένωσης. Μετά από 3 χρόνια, το πλεονέκτημα του SPS όσον αφορά τη μείωση της ανάγκης για επαναλαμβανόμενη επαναγγείωση λόγω υποτροπιάζουσας επαναστένωσης του stent παρέμεινε (19 έναντι 28,4%). Δεν υπήρξε σημαντική διαφορά στη συχνότητα εμφάνισης θρόμβωσης μεταξύ των ομάδων.
Οι κύριοι παράγοντες για την ανάπτυξη υποτροπιάζοντος VRS σε ασθενείς με LES στην περίπτωση εμφύτευσης SPS είναι η μικρή διάμετρος του αγγείου (< 2,5 mm), ο διάχυτος τύπος επαναστένωσης και η παρουσία χρόνιας νεφρικής ανεπάρκειας που απαιτεί αιμοκάθαρση. Στην τυχαιοποιημένη μελέτη TAXUS V ISR, η SPS επέδειξε επίσης υψηλή αποτελεσματικότητα στη θεραπεία του VRS, μειώνοντας το ποσοστό υποτροπιάζουσας επαναστένωσης κατά 54% σε σύγκριση με τη βραχυθεραπεία.
Διεξήχθησαν επίσης τυχαιοποιημένες δοκιμές που συνέκριναν την αποτελεσματικότητα της TBCA για την εμφύτευση VRS και DES. Στην τυχαιοποιημένη δοκιμή RIBS-II, μετά από 9 μήνες, η επαναλαμβανόμενη επαναστένωση ήταν 72% λιγότερο συχνή μετά την εμφύτευση DES σε σχέση με την TBCA, γεγονός που μείωσε την ανάγκη για επαναλαμβανόμενη επαναγγείωση από 30 σε 11%. Η δοκιμή ISAR DESIRE συνέκρινε την αποτελεσματικότητα της TBCA για την VRS με την εμφύτευση SPP ή SPS. Μετά από 6 μήνες, αποδείχθηκε ότι και οι δύο DES ήταν πιο αποτελεσματικές στην πρόληψη επαναλαμβανόμενης επαναστένωσης από την TBCA (η συχνότητά της ήταν 44,6% με την TBCA, 14,3% στην ομάδα SPS και 21,7% στην ομάδα SPS), γεγονός που μείωσε την ανάγκη για επαναλαμβανόμενη επαναγγείωση. Σε μια άμεση σύγκριση της SPP και της SPS, διαπιστώθηκε ότι η SPS μείωσε την ανάγκη για επαναλαμβανόμενη επαναγγείωση σημαντικά πιο αποτελεσματικά από την SPP (8 έναντι 19%). Έτσι, η εμφύτευση DES μειώνει τη συχνότητα εμφάνισης υποτροπιάζοντος LES VRS σε σύγκριση με την TBCA και τη βραχυθεραπεία, γεγονός που μειώνει τον αριθμό των επαναλαμβανόμενων PCI και ως εκ τούτου καθιστά την εμφύτευσή τους τη διαδικασία εκλογής σε αυτούς τους ασθενείς.
Επαναστένωση μετά από εμφύτευση stent που εκλούει φάρμακο (DES)
Παρά τη μείωση κατά 70-80% στη συχνότητα εμφάνισης στένωσης εντός του stent κατά τη χρήση DES σε σύγκριση με τον LES, δεν μπόρεσαν να αποκλείσουν εντελώς την ανάπτυξη αυτής της ιατρογενούς συνέπειας της τοποθέτησης stent. Η συνολική συχνότητα εμφάνισης παραμένει κατά μέσο όρο μικρότερη από 10%. Εκτός από την ποσοτική μείωση στη συχνότητα εμφάνισης επαναστένωσης, άλλαξαν επίσης σημαντικά τον τύπο επαναστένωσης που εμφανίζεται. Έτσι, μετά την εμφύτευση DES, η επαναστένωση είναι συνήθως εστιακή. Κλινικά, όπως και στην περίπτωση του LES, εκδηλώνεται συχνότερα ως υποτροπή σταθερής στηθάγχης (77%), λιγότερο συχνά (8%) είναι ασυμπτωματική. Στο 5% των περιπτώσεων, εκδηλώνεται ως ασταθής στηθάγχη και στο 10%, το πρώτο σύμπτωμα είναι το έμφραγμα του μυοκαρδίου χωρίς κύμα Q. Οι κύριοι παράγοντες στην ανάπτυξη επαναστένωσης DES είναι ο σακχαρώδης διαβήτης τύπου 2, η μικρή διάμετρος αγγείου και η έκταση της βλάβης. Δεν υπάρχουν σαφείς συστάσεις για τη διαχείριση τέτοιων ασθενών. Εναλλακτικές επιλογές είναι η επανεμφύτευση ενός DES (του ίδιου τύπου ή διαφορετικού), η TBCA ή η βραχυθεραπεία. Το μέσο ποσοστό επαναστένωσης με δεύτερη DES είναι 24% και είναι το ίδιο είτε εμφυτεύεται ο ίδιος τύπος DES είτε διαφορετικός.


 [
[