Νέες δημοσιεύσεις
Το σύστημα χορήγησης φαρμάκων κλειστού βρόχου θα μπορούσε να βελτιώσει τη χορήγηση χημειοθεραπείας
Τελευταία επισκόπηση: 02.07.2025

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.
Όταν οι ασθενείς με καρκίνο υποβάλλονται σε χημειοθεραπεία, οι δόσεις των περισσότερων φαρμάκων υπολογίζονται με βάση την επιφάνεια σώματος του ασθενούς. Αυτή η εκτίμηση γίνεται χρησιμοποιώντας μια εξίσωση που λαμβάνει υπόψη το ύψος και το βάρος του ασθενούς. Αυτή η εξίσωση διατυπώθηκε το 1916 με βάση δεδομένα από μόλις εννέα ασθενείς.
Αυτή η απλοποιημένη προσέγγιση στη δοσολογία δεν λαμβάνει υπόψη άλλους παράγοντες και μπορεί να οδηγήσει στη χορήγηση υπερβολικής ή ελάχιστης ποσότητας φαρμάκου σε έναν ασθενή. Ως αποτέλεσμα, ορισμένοι ασθενείς μπορεί να εμφανίσουν περιττή τοξικότητα ή ανεπαρκή αποτελεσματικότητα από τη χημειοθεραπεία που λαμβάνουν.
Για να βελτιώσουν την ακρίβεια της δοσολογίας της χημειοθεραπείας, οι μηχανικοί του MIT έχουν αναπτύξει μια εναλλακτική προσέγγιση που επιτρέπει την εξατομίκευση της δόσης για κάθε ασθενή. Το σύστημά τους μετρά την ποσότητα του φαρμάκου στο σώμα του ασθενούς και τροφοδοτεί αυτά τα δεδομένα σε έναν ελεγκτή που μπορεί να προσαρμόσει ανάλογα τον ρυθμό έγχυσης.
Αυτή η προσέγγιση θα μπορούσε να βοηθήσει στην αντιστάθμιση των διαφορών στη φαρμακοκινητική των φαρμάκων που προκαλούνται από τη σύνθεση του σώματος, τη γενετική προδιάθεση, την τοξικότητα οργάνων που προκαλείται από τη χημειοθεραπεία, τις αλληλεπιδράσεις με άλλα φάρμακα και τρόφιμα και τις κιρκαδικές διακυμάνσεις στα ένζυμα που είναι υπεύθυνα για τη διάσπαση των χημειοθεραπευτικών φαρμάκων, λένε οι ερευνητές.
«Αναγνωρίζοντας τις προόδους στην κατανόηση του τρόπου με τον οποίο μεταβολίζονται τα φάρμακα και εφαρμόζοντας εργαλεία μηχανικής για την απλοποίηση της εξατομικευμένης δοσολογίας, πιστεύουμε ότι μπορούμε να συμβάλουμε στον μετασχηματισμό της ασφάλειας και της αποτελεσματικότητας πολλών φαρμάκων», δήλωσε ο Giovanni Traverso, αναπληρωτής καθηγητής μηχανολογίας στο MIT, γαστρεντερολόγος στο Brigham and Women's Hospital και κύριος συγγραφέας της μελέτης.
Ο Louis DeRidder, μεταπτυχιακός φοιτητής στο MIT, είναι ο κύριος συγγραφέας της εργασίας που δημοσιεύτηκε στο περιοδικό Med.
Συνεχής παρακολούθηση
Σε αυτήν τη μελέτη, οι ερευνητές επικεντρώθηκαν σε ένα φάρμακο που ονομάζεται 5-φθοροουρακίλη, το οποίο χρησιμοποιείται για τη θεραπεία του καρκίνου του παχέος εντέρου και άλλων μορφών καρκίνου. Το φάρμακο χορηγείται συνήθως σε διάστημα 46 ωρών και η δοσολογία του καθορίζεται χρησιμοποιώντας έναν τύπο που βασίζεται στο ύψος και το βάρος του ασθενούς, ο οποίος δίνει μια εκτίμηση της επιφάνειας σώματος.
Ωστόσο, αυτή η προσέγγιση δεν λαμβάνει υπόψη τις διαφορές στη σύνθεση του σώματος που μπορούν να επηρεάσουν τον τρόπο με τον οποίο το φάρμακο κατανέμεται στο σώμα ή τις γενετικές παραλλαγές που επηρεάζουν τον τρόπο με τον οποίο μεταβολίζεται. Αυτές οι διαφορές μπορούν να οδηγήσουν σε επιβλαβείς παρενέργειες εάν χορηγηθεί υπερβολική δόση φαρμάκου. Εάν δεν χορηγηθεί αρκετή δόση φαρμάκου, μπορεί να μην σκοτώσει τον όγκο όπως αναμένεται.
«Άτομα με την ίδια επιφάνεια σώματος μπορεί να έχουν πολύ διαφορετικά ύψη και βάρη, διαφορετική μυϊκή μάζα ή διαφορετική γενετική, αλλά εφόσον το ύψος και το βάρος που ενσωματώνονται σε αυτήν την εξίσωση αποδίδουν την ίδια επιφάνεια σώματος, η δόση τους είναι πανομοιότυπη», λέει ο DeRidder, υποψήφιος διδάκτορας στο πρόγραμμα ιατρικής μηχανικής και ιατρικής φυσικής στο Πρόγραμμα Επιστημών Υγείας και Τεχνολογίας του Harvard-MIT.
Ένας άλλος παράγοντας που μπορεί να μεταβάλει την ποσότητα του φαρμάκου στο αίμα σε οποιαδήποτε δεδομένη στιγμή είναι η κιρκαδική διακύμανση σε ένα ένζυμο που ονομάζεται διυδροπυριμιδινική αφυδρογονάση (DPD), το οποίο διασπά την 5-φθοροουρακίλη. Η έκφραση της DPD, όπως και πολλά άλλα ένζυμα στο σώμα, ρυθμίζεται από έναν κιρκάδιο ρυθμό. Έτσι, η αποικοδόμηση της 5-FU από την DPD δεν είναι σταθερή, αλλά ποικίλλει ανάλογα με την ώρα της ημέρας. Αυτοί οι κιρκάδιοι ρυθμοί μπορούν να οδηγήσουν σε δεκαπλάσια διακύμανση στην ποσότητα της 5-FU στο αίμα ενός ασθενούς κατά τη διάρκεια μιας έγχυσης.
«Χρησιμοποιώντας την επιφάνεια του σώματος για τον υπολογισμό της δόσης χημειοθεραπείας, γνωρίζουμε ότι δύο άτομα μπορούν να έχουν πολύ διαφορετικές τοξικότητες από την 5-φθοροουρακίλη. Ένας ασθενής μπορεί να έχει κύκλους θεραπείας με ελάχιστη τοξικότητα και στη συνέχεια έναν κύκλο με τρομερή τοξικότητα. Κάτι έχει αλλάξει στον τρόπο με τον οποίο ο ασθενής μεταβολίζει τη χημειοθεραπεία από τον έναν κύκλο στον επόμενο. Η ξεπερασμένη μέθοδος δοσολογίας μας δεν καταγράφει αυτές τις αλλαγές και οι ασθενείς υποφέρουν ως αποτέλεσμα», λέει ο Douglas Rubinson, κλινικός ογκολόγος στο Dana-Farber Cancer Institute και συγγραφέας της μελέτης.
Ένας τρόπος για να αντισταθμιστεί η μεταβλητότητα στη φαρμακοκινητική της χημειοθεραπείας είναι μια στρατηγική που ονομάζεται θεραπευτική παρακολούθηση φαρμάκων, κατά την οποία ο ασθενής δίνει ένα δείγμα αίματος στο τέλος ενός κύκλου θεραπείας. Αφού αναλυθεί αυτό το δείγμα για συγκεντρώσεις φαρμάκου, η δοσολογία μπορεί να προσαρμοστεί, εάν είναι απαραίτητο, στην αρχή του επόμενου κύκλου (συνήθως δύο εβδομάδες για την 5-φθοροουρακίλη).
Αυτή η προσέγγιση έχει αποδειχθεί ότι οδηγεί σε καλύτερα αποτελέσματα για τους ασθενείς, αλλά δεν έχει χρησιμοποιηθεί ευρέως για χημειοθεραπείες όπως η 5-φθοροουρακίλη.
Οι ερευνητές του MIT ήθελαν να αναπτύξουν ένα παρόμοιο είδος παρακολούθησης, αλλά με αυτοματοποιημένο τρόπο που θα επέτρεπε την εξατομίκευση της δοσολογίας των φαρμάκων σε πραγματικό χρόνο, κάτι που θα μπορούσε να οδηγήσει σε καλύτερα αποτελέσματα για τους ασθενείς.
Στο σύστημα κλειστού βρόχου τους, οι συγκεντρώσεις φαρμάκων μπορούν να παρακολουθούνται συνεχώς και αυτές οι πληροφορίες χρησιμοποιούνται για την αυτόματη προσαρμογή του ρυθμού έγχυσης του χημειοθεραπευτικού φαρμάκου, ώστε να διατηρείται η δόση εντός του εύρους-στόχου.
Αυτό το σύστημα κλειστού βρόχου επιτρέπει την εξατομίκευση της δοσολογίας των φαρμάκων, λαμβάνοντας υπόψη τους κιρκαδικούς ρυθμούς των επιπέδων των ενζύμων που μεταβολίζουν τα φάρμακα, καθώς και τυχόν αλλαγές στη φαρμακοκινητική του ασθενούς από την τελευταία θεραπεία, όπως η τοξικότητα οργάνων που προκαλείται από τη χημειοθεραπεία.
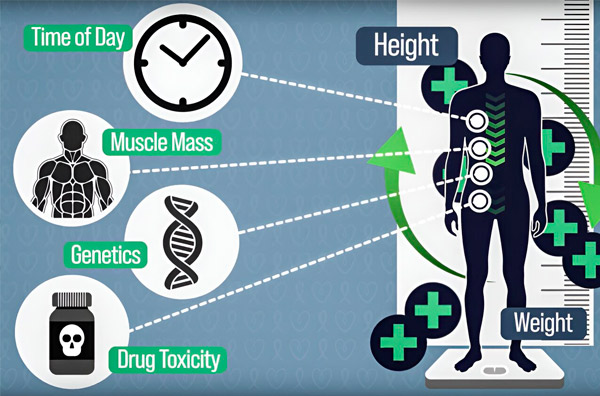
Για να κάνουν τη δοσολογία της χημειοθεραπείας πιο ακριβή, οι μηχανικοί του MIT ανέπτυξαν έναν τρόπο συνεχούς μέτρησης της ποσότητας του φαρμάκου στο σώμα ενός ασθενούς κατά τη διάρκεια μιας έγχυσης πολλών ωρών. Αυτό θα βοηθήσει στην αντιστάθμιση των διαφορών που προκαλούνται από τη σύνθεση του σώματος, τη γενετική, την τοξικότητα των φαρμάκων και τις κιρκαδικές ταλαντώσεις. Πηγή: Ευγενική προσφορά των ερευνητών.
Το νέο σύστημα που ανέπτυξαν οι ερευνητές, γνωστό ως CLAUDIA (Closed-Loop AUtomated Drug Infusion regulAtor), χρησιμοποιεί εμπορικά διαθέσιμο εξοπλισμό για κάθε βήμα. Λαμβάνονται δείγματα αίματος κάθε πέντε λεπτά και προετοιμάζονται γρήγορα για ανάλυση. Η συγκέντρωση της 5-φθοροουρακίλης στο αίμα μετριέται και συγκρίνεται με το εύρος-στόχο.
Η διαφορά μεταξύ της στοχευόμενης και της μετρούμενης συγκέντρωσης εισάγεται σε έναν αλγόριθμο ελέγχου, ο οποίος στη συνέχεια προσαρμόζει τον ρυθμό έγχυσης όπως απαιτείται για να διατηρήσει τη δόση εντός του εύρους των συγκεντρώσεων στις οποίες το φάρμακο είναι αποτελεσματικό και μη τοξικό.
«Έχουμε αναπτύξει ένα σύστημα όπου μπορούμε να μετράμε συνεχώς τη συγκέντρωση του φαρμάκου και να προσαρμόζουμε ανάλογα τον ρυθμό έγχυσης για να διατηρούμε τη συγκέντρωση του φαρμάκου στο θεραπευτικό παράθυρο», λέει ο DeRidder.
Γρήγορη προσαρμογή
Σε δοκιμές σε ζώα, οι ερευνητές διαπίστωσαν ότι χρησιμοποιώντας το CLAUDIA μπορούσαν να διατηρήσουν την ποσότητα του φαρμάκου που κυκλοφορεί στον οργανισμό εντός του εύρους-στόχου περίπου στο 45% του χρόνου.
Τα επίπεδα φαρμάκων σε ζώα που έλαβαν χημειοθεραπεία χωρίς CLAUDIA παρέμειναν εντός του εύρους-στόχου μόνο στο 13% του χρόνου κατά μέσο όρο. Οι ερευνητές δεν εξέτασαν την αποτελεσματικότητα των επιπέδων φαρμάκων σε αυτή τη μελέτη, αλλά η διατήρηση των συγκεντρώσεων στο παράθυρο-στόχο θεωρείται ότι οδηγεί σε καλύτερα αποτελέσματα και λιγότερη τοξικότητα.
Η CLAUDIA κατάφερε επίσης να διατηρήσει τη δόση 5-φθοροουρακίλης εντός του εύρους-στόχου, ακόμη και όταν χορηγήθηκε φάρμακο που αναστέλλει το ένζυμο DPD. Σε ζώα που έλαβαν αυτόν τον αναστολέα χωρίς συνεχή παρακολούθηση και προσαρμογή, τα επίπεδα 5-φθοροουρακίλης αυξήθηκαν έως και οκταπλάσια.
Για αυτήν την επίδειξη, οι ερευνητές εκτέλεσαν χειροκίνητα κάθε βήμα της διαδικασίας χρησιμοποιώντας έτοιμο εξοπλισμό, αλλά τώρα σχεδιάζουν να αυτοματοποιήσουν κάθε βήμα, έτσι ώστε η παρακολούθηση και οι προσαρμογές της δόσης να μπορούν να γίνονται χωρίς ανθρώπινη παρέμβαση.
Για τη μέτρηση των συγκεντρώσεων φαρμάκων, οι ερευνητές χρησιμοποίησαν υγρή χρωματογραφία υψηλής απόδοσης-φασματομετρία μάζας (HPLC-MS), μια τεχνική που μπορεί να προσαρμοστεί για την ανίχνευση σχεδόν οποιουδήποτε τύπου φαρμάκου.
«Βλέπουμε ένα μέλλον όπου μπορούμε να χρησιμοποιήσουμε το CLAUDIA για οποιοδήποτε φάρμακο που έχει τις κατάλληλες φαρμακοκινητικές ιδιότητες και είναι ανιχνεύσιμο με HPLC-MS, επιτρέποντας την εξατομικευμένη δοσολογία για πολλά διαφορετικά φάρμακα», λέει ο DeRidder.
