Νέες δημοσιεύσεις
Παράγωγα ενώσεων θαλιδομίδης οδηγούν στο θάνατο ανθεκτικών καρκινικών κυττάρων
Τελευταία επισκόπηση: 02.07.2025

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.
Μια μελέτη που διεξήχθη από το Πανεπιστήμιο Γκαίτε στη Φρανκφούρτη υποδεικνύει την πιθανότητα τα παράγωγα της θαλιδομίδης να μπορούν να χρησιμοποιηθούν για τη θεραπεία του καρκίνου. Η θαλιδομίδη πωλούνταν ως υπνωτικό χάπι τη δεκαετία του 1950. Αργότερα έγινε διαβόητη για την πρόκληση σοβαρών γενετικών ανωμαλιών στα πρώτα στάδια της εγκυμοσύνης.
Το μόριο είναι επίσης γνωστό ότι σηματοδοτεί πρωτεΐνες στο κύτταρο για καταστροφή. Στο πλαίσιο της τρέχουσας μελέτης, οι επιστήμονες δημιούργησαν παράγωγα της θαλιδομίδης. Κατάφεραν να δείξουν ότι αυτές οι ουσίες επηρεάζουν την καταστροφή πρωτεϊνών που είναι υπεύθυνες για την επιβίωση των καρκινικών κυττάρων.
Ίσως κανένα άλλο μόριο δεν είχε τόσο ταραχώδες παρελθόν όσο η θαλιδομίδη. Ήταν το κύριο συστατικό ενός φαρμάκου που εγκρίθηκε σε πολλές χώρες τη δεκαετία του 1950 ως ηρεμιστικό και υπνωτικό χάπι. Σύντομα όμως έγινε σαφές ότι οι έγκυες γυναίκες που έπαιρναν θαλιδομίδη συχνά γεννούσαν μωρά με σοβαρές παραμορφώσεις.
Ωστόσο, τις τελευταίες δεκαετίες, η ιατρική έχει για άλλη μια φορά εναποθέσει μεγάλες ελπίδες σε αυτό. Μελέτες έχουν δείξει, μεταξύ άλλων, ότι αναστέλλει την ανάπτυξη των αιμοφόρων αγγείων και ως εκ τούτου είναι δυνητικά κατάλληλο για την αποκοπή των όγκων από το θρεπτικό τους μέσο. Στη συνέχεια, αποδείχθηκε επίσης πολύ αποτελεσματικό στη θεραπεία του πολλαπλού μυελώματος, κακοήθων όγκων στον μυελό των οστών.
«Γνωρίζουμε πλέον ότι η θαλιδομίδη μπορεί να ονομαστεί «μοριακή κόλλα»», εξηγεί ο Δρ Ξινγκλάι Τσενγκ του Ινστιτούτου Φαρμακευτικής Χημείας στο Πανεπιστήμιο Γκαίτε της Φρανκφούρτης. «Αυτό σημαίνει ότι είναι σε θέση να «αρπάξει» δύο πρωτεΐνες και να τις ενώσει».
Αυτό είναι ιδιαίτερα ενδιαφέρον επειδή μία από αυτές τις πρωτεΐνες είναι ένα είδος «μηχανής επισήμανσης»: προσκολλά μια σαφή ετικέτα «ΣΚΟΥΠΙΔΙΑ» σε μια άλλη πρωτεΐνη.
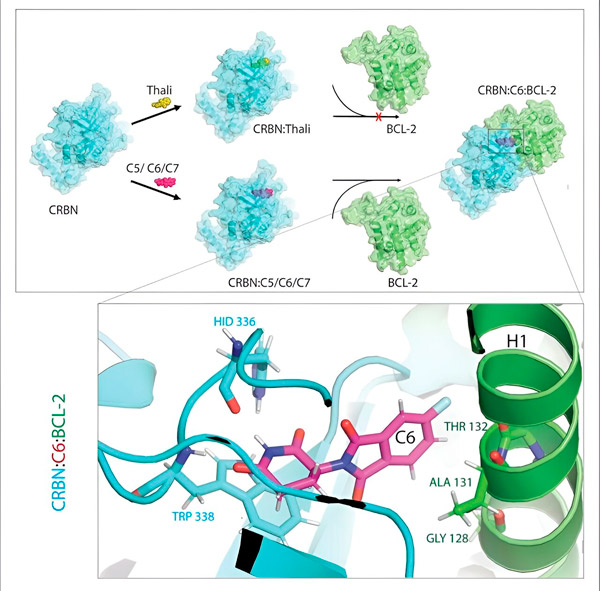
Τα παράγωγα της θαλιδομίδης C5, C6 και C7 τροποποιούν την CRBN, τη «μηχανή σήμανσης», έτσι ώστε να μπορεί να συνδεθεί με την BCL-2. Με αυτόν τον τρόπο, το μόριο BCL-2 σημαδεύεται για αποικοδόμηση — μια πιθανή νέα στρατηγική για την καταπολέμηση του καρκίνου. Συγγραφέας: Δρ. Xinglai Cheng.
Το σύστημα απόρριψης αποβλήτων του κυττάρου αναγνωρίζει αυτήν την ετικέτα: Αρπάζει το σημασμένο μόριο πρωτεΐνης και το καταστρέφει. «Αυτός ο μηχανισμός εξηγεί τις διαφορετικές επιδράσεις της θαλιδομίδης», λέει ο Cheng. «Ανάλογα με το ποια πρωτεΐνη είναι σημασμένη, μπορεί να προκαλέσει παραμορφώσεις κατά την εμβρυϊκή ανάπτυξη ή να καταστρέψει κακοήθη κύτταρα».
Αυτός ο μηχανισμός ανοίγει μεγάλες δυνατότητες για την ιατρική, καθώς τα καρκινικά κύτταρα εξαρτώνται από ορισμένες πρωτεΐνες για να επιβιώσουν. Αν μπορούσαν να στοχευθούν και να τεμαχιστούν συστηματικά, ίσως η ασθένεια να μπορούσε να θεραπευτεί. Το πρόβλημα είναι ότι η μοριακή κόλλα είναι αρκετά ιδιόμορφη.
Ένας από τους συνεργάτες σύνδεσής του είναι πάντα η μηχανή σήμανσης του κυττάρου ή, στην επιστημονική ορολογία, μια λιγάση Ε3 που ονομάζεται CRBN. Μόνο ελάχιστες από τις πολλές χιλιάδες πρωτεΐνες στο σώμα μπορούν να είναι ο δεύτερος συνεργάτης —ποιες από αυτές εξαρτώνται από την κόλλα.
«Έτσι, δημιουργήσαμε μια σειρά από παράγωγα θαλιδομίδης», λέει ο Cheng. «Στη συνέχεια, ελέγξαμε αν είχαν προσκολλητικές ιδιότητες και, αν ναι, έναντι ποιων πρωτεϊνών ήταν αποτελεσματικές». Για να το πετύχουν αυτό, οι ερευνητές πρόσθεσαν τα παράγωγά τους σε όλες τις πρωτεΐνες της καλλιεργημένης κυτταρικής σειράς. Στη συνέχεια, παρατήρησαν ποιες από αυτές τις πρωτεΐνες αποικοδομήθηκαν παρουσία CRBN.
«Κατά τη διάρκεια της διαδικασίας, εντοπίσαμε τρία παράγωγα που θα μπορούσαν να επισημάνουν μια κυτταρική πρωτεΐνη που είναι πολύ σημαντική για την αποικοδόμηση, την BCL-2», εξηγεί ο Cheng. «Η BCL-2 εμποδίζει τα κύτταρα να ενεργοποιήσουν το πρόγραμμα αυτοκαταστροφής τους, οπότε αν δεν υπάρχει, τα κύτταρα πεθαίνουν».
Γι' αυτό το λόγο, το BCL-2 αποτελεί εδώ και καιρό επίκεντρο της έρευνας για τον καρκίνο. Υπάρχει ακόμη και ένα φάρμακο για τη λευχαιμία που ονομάζεται venetoclax, το οποίο μειώνει την αποτελεσματικότητα του BCL-2 και έτσι προκαλεί την αυτοκαταστροφή των μεταλλαγμένων κυττάρων.
«Ωστόσο, σε πολλά καρκινικά κύτταρα, το ίδιο το BCL-2 μεταλλάσσεται. Ως αποτέλεσμα, το venetoclax δεν αναστέλλει πλέον την πρωτεΐνη», λέει ο Cheng. «Καταφέραμε να δείξουμε ότι τα παράγωγά μας επισημαίνουν επίσης αυτή τη μεταλλαγμένη μορφή για αποικοδόμηση. Επιπλέον, οι συνεργάτες μας στο Ινστιτούτο Βιοφυσικής Max Planck προσομοίωσαν την αλληλεπίδραση παραγώγων θαλιδομίδης με το BCL-2 σε έναν υπολογιστή. Αυτό έδειξε ότι τα παράγωγα συνδέονται σε εντελώς διαφορετικές θέσεις από το venetoclax - ένα αποτέλεσμα που αργότερα μπορέσαμε να επιβεβαιώσουμε πειραματικά».
Οι ερευνητές δοκίμασαν επίσης τις ενώσεις τους σε μύγες των φρούτων με καρκινικά κύτταρα. Το ποσοστό επιβίωσης των μυγών που αντιμετωπίστηκαν με αυτόν τον τρόπο ήταν σημαντικά υψηλότερο. Ωστόσο, ο Cheng προειδοποιεί να μην υπάρχουν υπερβολικές ελπίδες, καθώς αυτά τα αποτελέσματα εξακολουθούν να αποτελούν βασική έρευνα. «Ενώ δείχνουν ότι τα τροποποιημένα μόρια θαλιδομίδης έχουν μεγάλο θεραπευτικό δυναμικό, δεν μπορούμε ακόμη να πούμε αν θα αποδειχθούν αποτελεσματικά στην πράξη κάποια στιγμή».
Τα αποτελέσματα της μελέτης δημοσιεύθηκαν στο περιοδικό Cell Reports Physical Science.
