Νέες δημοσιεύσεις
Επιστήμονες ανακαλύπτουν νέο ανοσοκατασταλτικό μηχανισμό στον καρκίνο του εγκεφάλου
Τελευταία επισκόπηση: 02.07.2025

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.
Ο αναπληρωτής καθηγητής Filippo Veglia, Ph.D., και η ομάδα του στο Ινστιτούτο Wistar ανακάλυψαν έναν βασικό μηχανισμό μέσω του οποίου το γλοιοβλάστωμα - ένας σοβαρός και συχνά θανατηφόρος καρκίνος του εγκεφάλου - καταστέλλει το ανοσοποιητικό σύστημα, έτσι ώστε ο όγκος να μπορεί να αναπτυχθεί ανεμπόδιστος από τις άμυνες του οργανισμού.
Η ανακάλυψή τους δημοσιεύτηκε στο άρθρο με τίτλο «Glucose-driven histone lactylation promotes the immunosuppressive activity of monocyte-derived macrophages in glioblastoma» στο περιοδικό Immunity.
«Η μελέτη μας δείχνει ότι οι μηχανισμοί αυτοδιαιώνισης του καρκίνου, εάν κατανοηθούν επαρκώς, μπορούν να αξιοποιηθούν πολύ αποτελεσματικά κατά της νόσου», δήλωσε ο Δρ. Βέγλια.
«Προσβλέπω σε μελλοντικές μελέτες των μηχανισμών ανοσοκαταστολής που προκαλούνται από τον μεταβολισμό στο γλοιοβλάστωμα και ελπίζω ότι θα συνεχίσουμε να μαθαίνουμε περισσότερα για το πώς να κατανοούμε καλύτερα και να καταπολεμούμε αυτόν τον καρκίνο».
Μέχρι τώρα, λίγα έχουν μελετηθεί για το πώς τα μακροφάγα και η μικρογλοία που προέρχονται από μονοκύτταρα δημιουργούν ένα ανοσοκατασταλτικό μικροπεριβάλλον όγκου στο γλοιοβλάστωμα.
Το εργαστήριο Veglia διερεύνησε τους κυτταρικούς μηχανισμούς της ανοσοκαταστολής στο γλοιοβλάστωμα και διαπίστωσε ότι καθώς το γλοιοβλάστωμα εξελίσσεται, τα μακροφάγα που προέρχονται από μονοκύτταρα αρχίζουν να υπερτερούν αριθμητικά της μικρογλοίας, υποδηλώνοντας ότι η κυριαρχία των μακροφάγων που προέρχονται από μονοκύτταρα στο μικροπεριβάλλον του όγκου είναι ευεργετική για τον καρκίνο όσον αφορά την ανοσολογική αποφυγή.
Πράγματι, τα μακροφάγα που προέρχονται από μονοκύτταρα, αλλά όχι η μικρογλοία, μπλόκαραν τη δραστηριότητα των Τ κυττάρων (κυττάρων του ανοσοποιητικού συστήματος που σκοτώνουν τα καρκινικά κύτταρα) σε προκλινικά μοντέλα και σε ασθενείς. Η ομάδα επιβεβαίωσε αυτό αξιολογώντας προκλινικά μοντέλα γλοιοβλαστώματος με τεχνητά μειωμένο αριθμό μακροφάγων που προέρχονται από μονοκύτταρα.
Όπως αναμενόταν, τα μοντέλα με λιγότερα κακοήθη μακροφάγα στο μικροπεριβάλλον του όγκου έδειξαν βελτιωμένα αποτελέσματα σε σύγκριση με τα τυπικά μοντέλα γλοιοβλαστώματος.
Το γλοιοβλάστωμα ευθύνεται για λίγο περισσότερο από το ήμισυ όλων των κακοήθων όγκων που εμφανίζονται στον εγκέφαλο και η πρόγνωση για τους ασθενείς που διαγιγνώσκονται με τη νόσο είναι εξαιρετικά κακή: μόνο το 25% των ασθενών επιβιώνουν τον πρώτο χρόνο μετά τη διάγνωση. Το γλοιοβλάστωμα είναι επικίνδυνο όχι μόνο λόγω της θέσης του στον εγκέφαλο, αλλά και λόγω του ανοσοκατασταλτικού μικροπεριβάλλοντος του όγκου, το οποίο καθιστά το γλοιοβλάστωμα ανθεκτικό σε πολλά υποσχόμενες ανοσοθεραπείες.
Προγραμματίζοντας ορισμένα ανοσοκύτταρα, όπως τα μακροφάγα (μακροφάγα που προέρχονται από μονοκύτταρα και μικρογλοία), να εργάζονται για τον όγκο και όχι εναντίον του, το γλοιοβλάστωμα δημιουργεί ένα μικροπεριβάλλον όγκου για τον εαυτό του που επιτρέπει στον καρκίνο να αναπτύσσεται επιθετικά, αποφεύγοντας παράλληλα τις αντικαρκινικές ανοσολογικές αποκρίσεις.
Διευκρίνιση του μηχανισμού
Έχοντας επιβεβαιώσει τον ρόλο των μακροφάγων που προέρχονται από μονοκύτταρα, το εργαστήριο του Weglia προσπάθησε στη συνέχεια να κατανοήσει ακριβώς πώς αυτά τα ανοσοκύτταρα που σχετίζονται με τον καρκίνο λειτουργούν ενάντια στο ανοσοποιητικό σύστημα.
Ανέλυσαν την αλληλουχία των μακροφάγων για να προσδιορίσουν εάν τα κύτταρα είχαν τυχόν μη φυσιολογικά πρότυπα γονιδιακής έκφρασης που θα μπορούσαν να υποδηλώνουν γονίδια που παίζουν ρόλο στην ανοσοκαταστολή και εξέτασαν επίσης τα μεταβολικά πρότυπα των μακροφάγων για να δουν εάν η μη φυσιολογική γονιδιακή έκφραση σχετιζόταν με τον μεταβολισμό.
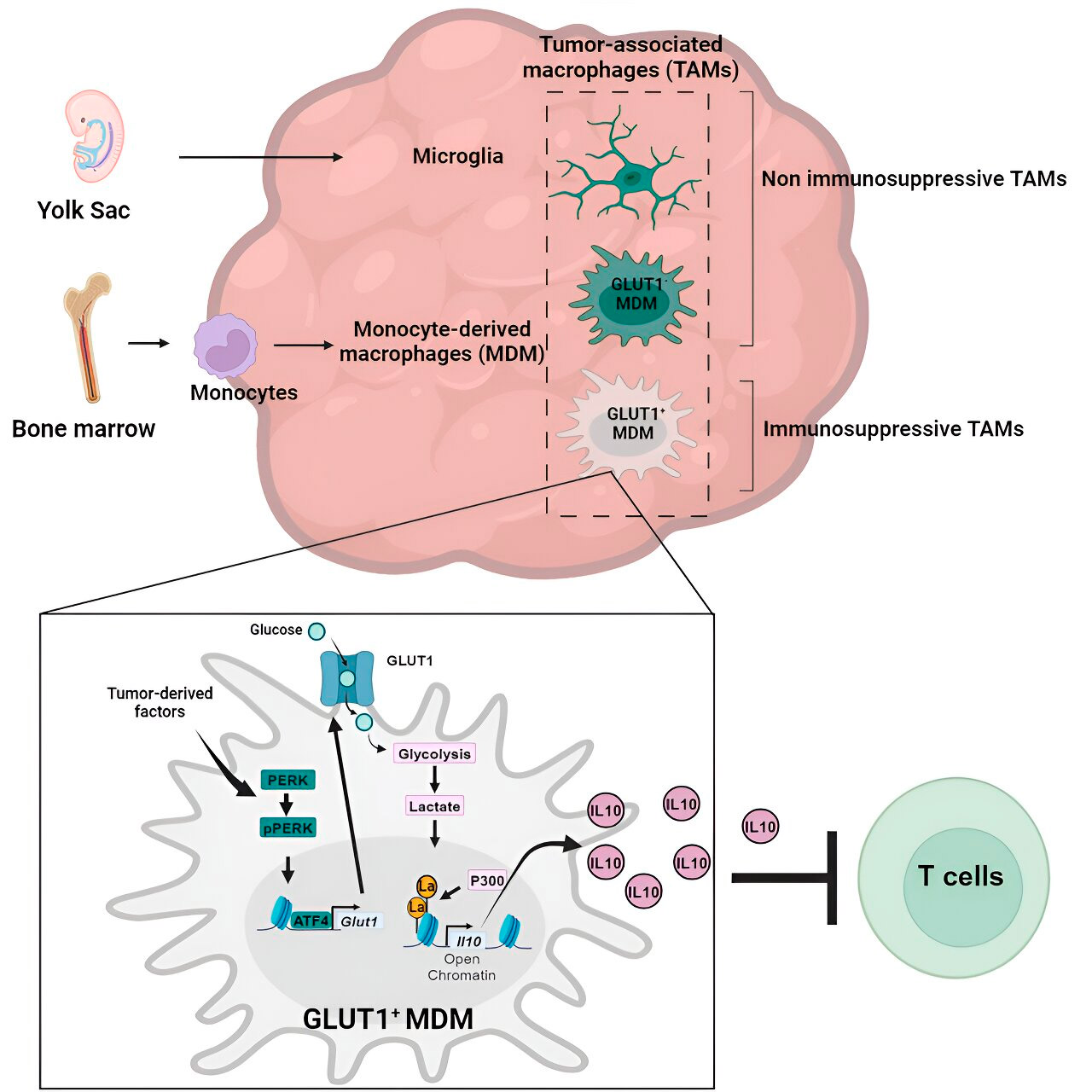
Η γονιδιακή και μεταβολική ανάλυση τους οδήγησε στον μεταβολισμό της γλυκόζης. Μια σειρά από δοκιμές έδειξε ότι τα μακροφάγα που προέρχονται από μονοκύτταρα με αυξημένο μεταβολισμό γλυκόζης και έκφραση GLUT1, του κύριου μεταφορέα γλυκόζης, μπλόκαραν τη λειτουργία των Τ-κυττάρων απελευθερώνοντας ιντερλευκίνη-10 (IL-10).
Η ομάδα απέδειξε ότι το γλοιοβλάστωμα διαταράσσει τον μεταβολισμό της γλυκόζης σε αυτά τα μακροφάγα, προκαλώντας την ανοσοκατασταλτική τους δράση.
Λακτυλίωση ιστονών και ο ρόλος της
Οι ερευνητές διαπίστωσαν ότι το κλειδί για την ανοσοκατασταλτική δράση των μακροφάγων που προέρχονται από μονοκύτταρα, η οποία σχετίζεται με τον μεταβολισμό της γλυκόζης, έγκειται σε μια διαδικασία που ονομάζεται «λακτυλίωση ιστονών». Οι ιστόνες είναι δομικές πρωτεΐνες στο γονιδίωμα που παίζουν βασικό ρόλο στην έκφραση γονιδίων όπως η IL-10 σε ορισμένα πλαίσια.
Με τον ταχύ μεταβολισμό της γλυκόζης, τα μακροφάγα που προέρχονται από μονοκύτταρα παράγουν γαλακτικό, ένα υποπροϊόν του μεταβολισμού της γλυκόζης. Οι ιστόνες μπορούν να «γαλακτυλιωθούν» (δηλαδή, το γαλακτικό ενσωματώνεται στις ιστόνες) με τέτοιο τρόπο ώστε η οργάνωση των ιστονών να προάγει την έκφραση της IL-10, η οποία παράγεται από μακροφάγα που προέρχονται από μονοκύτταρα για την υποστήριξη της ανάπτυξης καρκινικών κυττάρων.
Λύση στο πρόβλημα
Πώς όμως μπορεί να σταματήσει η ανοσοκατασταλτική δράση των μακροφάγων που προέρχονται από μονοκύτταρα και σχετίζονται με τον μεταβολισμό της γλυκόζης; Ο Δρ. Βέγλια και η ομάδα του εντόπισαν μια πιθανή λύση: το PERK, ένα ένζυμο που εντόπισαν ως ρυθμιστή του μεταβολισμού της γλυκόζης και της έκφρασης GLUT1 στα μακροφάγα.
Σε προκλινικά μοντέλα γλοιοβλαστώματος, η στόχευση του PERK διατάραξε τη λακτυλίωση των ιστονών και την ανοσοκατασταλτική δράση των μακροφάγων, και όταν συνδυάστηκε με ανοσοθεραπεία, μπλόκαρε την εξέλιξη του γλοιοβλαστώματος και προκάλεσε μακροχρόνια ανοσία που προστάτευσε τον εγκέφαλο από την επανεμφάνιση του όγκου, υποδηλώνοντας ότι η στόχευση του άξονα PERK-λακτυλίωσης ιστονών μπορεί να είναι μια βιώσιμη στρατηγική για την καταπολέμηση αυτού του θανατηφόρου καρκίνου του εγκεφάλου.
