Νέες δημοσιεύσεις
Ερευνητές εντοπίζουν μεταλλάξεις που προστατεύουν από τον καρκίνο των Β-κυττάρων
Τελευταία επισκόπηση: 02.07.2025

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.
Ερευνητές στο Ιατρικό Κέντρο Southwestern του Πανεπιστημίου του Τέξας κατάφεραν να καταστείλουν τη λευχαιμία και το λέμφωμα σε ένα μοντέλο ποντικού με γενετική προδιάθεση για αυτούς τους καρκίνους, εξαντλώντας πλήρως ή μερικώς μια πρωτεΐνη που ονομάζεται μιδνολίνη στα Β κύτταρα.
Τα ευρήματά τους, που δημοσιεύθηκαν στο Journal of Experimental Medicine, θα μπορούσαν να οδηγήσουν σε νέες θεραπείες για αυτές τις ασθένειες που θα αποφεύγουν τις σοβαρές παρενέργειες των τρεχουσών θεραπειών.
«Χρησιμοποιήσαμε μια καθαρά γενετική προσέγγιση για να βρούμε έναν φαρμακευτικό στόχο και αυτός ο στόχος ήταν εντυπωσιακός επειδή οι λευχαιμίες και τα λεμφώματα των Β-κυττάρων εξαρτώνται σε μεγάλο βαθμό από αυτόν, ενώ οι περισσότεροι ιστοί ξενιστή δεν εξαρτώνται», δήλωσε ο επικεφαλής της μελέτης Bruce Beutler, MD, διευθυντής του Κέντρου Γενετικής Άμυνας Ξενιστή και καθηγητής ανοσολογίας και εσωτερικής παθολογίας στο Ιατρικό Κέντρο Southwestern του Πανεπιστημίου του Τέξας.
Ο Δρ. Beutler, ο οποίος κέρδισε το βραβείο Νόμπελ Φυσιολογίας ή Ιατρικής το 2011 για την ανακάλυψη μιας σημαντικής ομάδας αισθητήρων παθογόνων, γνωστών ως υποδοχέων τύπου Toll, που βρίσκονται σε ανοσοκύτταρα, χρησιμοποιεί εδώ και καιρό τη μεταλλαξιογένεση - την εισαγωγή μεταλλάξεων στα γονίδια ζωικών μοντέλων μέσω έκθεσης σε μια χημική ουσία που ονομάζεται Ν-αιθυλ-Ν-νιτροζουρία (ENU) - ως βασικό εργαλείο για τη μελέτη της γονιδιακής λειτουργίας.
Πρόσφατα, το εργαστήριο του Beutler ανέπτυξε μια μέθοδο γνωστή ως αυτοματοποιημένη μειωτική χαρτογράφηση (AMM), η οποία ανιχνεύει ασυνήθιστα χαρακτηριστικά σε μεταλλαγμένα ποντίκια μέχρι τις αιτιολογικές μεταλλάξεις, εντοπίζοντας έτσι γονίδια που είναι απαραίτητα για τη διατήρηση της φυσιολογικής κατάστασης.
Η μεταλλαξιογένεση συχνά προκαλεί γενετικές ασθένειες στα ζώα, παρέχοντας πληροφορίες για τη λειτουργία των προσβεβλημένων γονιδίων μελετώντας ανωμαλίες στα ζώα. Ωστόσο, όπως εξήγησε ο Δρ. Μπόιτλερ, οι μεταλλάξεις μπορούν επίσης να παρέχουν προστασία από ασθένειες.
Παραδείγματα περιλαμβάνουν μεταλλάξεις που προστατεύουν άτομα με HIV ή κληρονομική δρεπανοκυτταρική αναιμία από την εμφάνιση συμπτωμάτων. Οι μηχανισμοί που διέπουν ορισμένες προστατευτικές μεταλλάξεις έχουν εμπνεύσει την ανάπτυξη φαρμάκων για τη θεραπεία μιας ποικιλίας ασθενειών.
Αναζητώντας προστατευτικές μεταλλάξεις για ανοσολογικές διαταραχές, οι ερευνητές εξέτασαν μεταλλαγμένα ποντίκια για ανοσοκύτταρα με ασυνήθιστα χαρακτηριστικά. Σε αρκετές ομάδες ζώων με ασυνήθιστα χαμηλό αριθμό Β κυττάρων - ένα σημαντικό συστατικό του προσαρμοστικού ανοσοποιητικού συστήματος που είναι υπεύθυνο για την παραγωγή αντισωμάτων - οι ερευνητές χρησιμοποίησαν την AMM για να εντοπίσουν την ανεπάρκεια σε μεταλλάξεις στη μιδνολίνη, μια πρωτεΐνη που βρίσκεται κυρίως στα Β κύτταρα.
Αν και τα ζώα που δεν έχουν καθόλου μιδνολίνη πεθαίνουν κατά την ανάπτυξη πριν από τη γέννηση, οι ηπιότερες μεταλλάξεις, συμπεριλαμβανομένων ορισμένων που εισάγονται μέσω γενετικών τεχνικών που επιτρέπουν τη διαγραφή του γονιδίου κατά την ενηλικίωση, δεν προκαλούν εμφανή βλάβη.
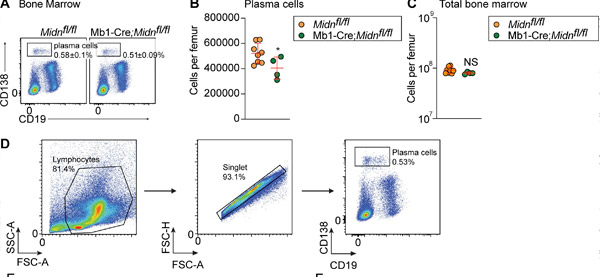
Παραγωγή πλασματοκυττάρων μετά από ανοσοποίηση με το αντιγόνο β-γαλακτοσιδάσης TD σε ποντίκια Mb1-Cre;Midn fl/fl. (A και B) Αντιπροσωπευτικά γραφήματα κυτταρομετρίας ροής (A) και αριθμοί (B) πλασματοκυττάρων στον μυελό των οστών ποντικών Mb1-Cre;Midn fl/fl και Midn fl/fl ηλικίας 8 εβδομάδων μετά από ανοσοποίηση με β-γαλακτοσιδάση. (C) Συνολικά κύτταρα μυελού των οστών ανά μηριαίο οστό. (D) Στρατηγική απομόνωσης πλασματοκυττάρων. Πηγή: Journal of Experimental Medicine (2024). DOI: 10.1084/jem.20232132
Οι ερευνητές μείωσαν σημαντικά ή εξάλειψαν τη μιδνολίνη σε ποντίκια με γενετική προδιάθεση για λευχαιμία και λέμφωμα Β-κυττάρων, καρκίνους στους οποίους τα Β κύτταρα διαιρούνται ανεξέλεγκτα. Αν και τα ποντίκια με φυσιολογικά επίπεδα μιδνολίνης πέθαναν από αυτές τις ασθένειες στους 5 μήνες, τα περισσότερα από αυτά με λιγότερη ή καθόλου μιδνολίνη δεν ανέπτυξαν ποτέ κακοήθεις όγκους.
Πρόσθετα πειράματα έδειξαν ότι ο ρόλος της μιδνολίνης στα Β κύτταρα είναι η διέγερση της δραστηριότητας των πρωτεασωμάτων, κυτταρικών οργανιδίων που απορρίπτουν τις κατεστραμμένες ή μη απαραίτητες πρωτεΐνες. Ορισμένες θεραπείες που χρησιμοποιούνται σήμερα για τη θεραπεία της λευχαιμίας και του λεμφώματος των Β κυττάρων λειτουργούν αναστέλλοντας τη δραστηριότητα του πρωτεασώματος, όπως ακριβώς κάνει η αφαίρεση της μιδνολίνης, εξήγησε ο Δρ. Beutler.
Ωστόσο, σε αντίθεση με αυτά τα φάρμακα, τα οποία έχουν πολλές δυνητικά σοβαρές παρενέργειες, η εξάλειψη ή η μείωση της μιδνολίνης σε ζωικά μοντέλα δεν φάνηκε να έχει αρνητικές επιπτώσεις.
Η μελλοντική έρευνα θα επικεντρωθεί στην ανάπτυξη φαρμάκων που αναστέλλουν τη μιδνολίνη, η οποία μπορεί τελικά να αποτελέσει τη βάση για νέες θεραπείες για τον καρκίνο των Β-κυττάρων.
