Η μελέτη υπογραμμίζει την ανάγκη για κυτταρικού τύπου θεραπείες για τον HIV
Τελευταία επισκόπηση: 14.06.2024

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.
Ερευνητές από το Πανεπιστήμιο του Ιλινόις έχουν αποδείξει τη σημασία της στόχευσης συγκεκριμένων τύπων κυττάρων στη θεραπεία του HIV. Η μελέτη τους, που δημοσιεύτηκε στο Proceedings of the National Academy of Sciences, είναι μία από τις πρώτες που εξέτασε τις διαφορικές ή κυτταροειδικές επιδράσεις της τροποποίησης του λανθάνοντος χρόνου του HIV στα μυελοειδή κύτταρα.. Κύτταρα, ένας τύπος ανοσοκυττάρου που παράγεται στον μυελό των οστών.
Ένα από τα σημαντικότερα εμπόδια για την εξάλειψη της λοίμωξης HIV είναι η διαχείριση του λανθάνοντος χρόνου ή η περίοδος κατά την οποία ένα μολυσμένο κύτταρο παραμένει αδρανές και δεν μπορεί να παράγει ιό. Τα λανθάνοντα κύτταρα HIV συγκεντρώνονται στο σώμα σε μέρη γνωστά ως δεξαμενές. Οι λανθάνουσες δεξαμενές είναι προβληματικές επειδή μπορούν να αρχίσουν να παράγουν ιούς ανά πάσα στιγμή.
Η πλήρης εκρίζωση της νόσου θα απαιτήσει την αφαίρεση όλων των λανθάνοντων κυττάρων από το σώμα ή τη μόνιμη αντίσταση στα ερεθίσματα ενεργοποίησης. Ωστόσο, η επανενεργοποίηση μπορεί να προκληθεί από διάφορους παράγοντες, συμπεριλαμβανομένων των σημάτων που κατευθύνουν τη διαφοροποίηση των μυελοειδών κυττάρων.
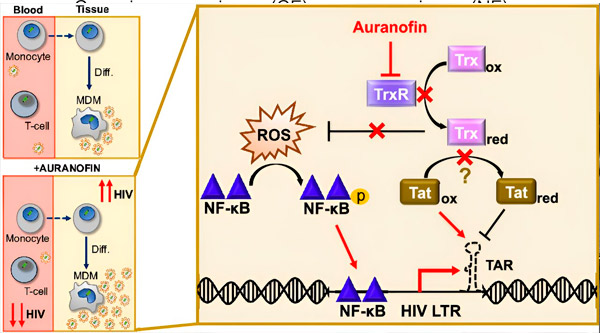
Η ρύθμιση της λανθάνουσας κατάστασης του HIV σε μακροφάγα που προέρχονται από μονοκύτταρα (MDM) μπορεί να ενέχει κίνδυνο για εξάπλωση του ιού. Η διαφοροποίηση των μονοκυττάρων σε μακροφάγα μπορεί να προκαλέσει επανενεργοποίηση του HIV, προάγοντας δυνητικά την εξάπλωση του ιού στους ιστούς (πάνω αριστερά). Το κλινικό υποψήφιο, το Auranofin, μειώνει το DNA του ιού στο αίμα και προάγει τον λανθάνοντα χρόνο του HIV σε Τ κύτταρα και μονοκύτταρα, αλλά προκαλεί επανενεργοποίηση του HIV στο MDM (κάτω αριστερά). Στο MDM, υποθέτουμε ότι η αναστολή του TrxR από το Auranofin οδηγεί στη συσσώρευση αντιδραστικών ειδών οξυγόνου (ROS), που προκαλεί ενεργοποίηση NF-κB και ενεργοποίηση του προαγωγέα HIV LTR (δεξιά). Η αναστολή του TrxR δυνητικά μειώνει τη μείωση του υποστρώματος επιτρέποντας στην πρωτεΐνη Tat να παραμείνει κυρίως οξειδωμένη, όπου μπορεί να συνδεθεί με το TAR και να ξεκινήσει τη μεταγραφή του HIV. Πηγή: Proceedings of the National Academy of Sciences (2024). DOI: 10.1073/pnas.2313823121
Για πολλά χρόνια, η έρευνα για μια θεραπεία για τον HIV επικεντρώνεται σε δύο προσεγγίσεις γνωστές ως "shock and kill" και "block and lock". Η πρώτη λειτουργεί σε συνδυασμό με αντιρετροϊκή θεραπεία για να ενεργοποιήσει λανθάνοντα μολυσμένα κύτταρα και να τα σκοτώσει μέσω απόπτωσης ή προγραμματισμένου κυτταρικού θανάτου, ενώ η δεύτερη αναγκάζει τα μολυσμένα κύτταρα να εισέλθουν σε μια βαθιά λανθάνουσα κατάσταση από την οποία δεν μπορούν να επανενεργοποιηθούν μόνα τους.
Η έρευνα γύρω από αυτές τις τεχνικές έχει παραδοσιακά επικεντρωθεί σε έναν τύπο λευκών αιμοσφαιρίων που ονομάζονται Τ κύτταρα, τα οποία είναι ο κύριος στόχος της μόλυνσης από τον ιό HIV. Ωστόσο, οι λανθάνουσες δεξαμενές δεν αποτελούνται αποκλειστικά από Τ κύτταρα. Στην πραγματικότητα, περιέχουν δεκάδες διαφορετικούς τύπους κυττάρων, ο καθένας με τα δικά του μοναδικά πρότυπα έκφρασης του γονιδίου HIV.
"Υπάρχει τεράστια ποικιλομορφία κυττάρων, ακόμη και μέσα σε μία μόνο γενεαλογία", δήλωσε ο Collin Kieffer, επίκουρος καθηγητής μικροβιολογίας και συγγραφέας της εργασίας. "Η μεταβλητότητα στην απόκριση σε αυτές τις δεξαμενές αυξάνεται με κάθε νέο τύπο κυττάρου."
Η Alexandra Blanco, μεταπτυχιακή φοιτήτρια στο εργαστήριο του Kieffer, ήθελε να μελετήσει τύπους κυττάρων που είχαν χάσει στην παραδοσιακή έρευνα για τον HIV. Εστιάζοντας στα μυελοειδή κύτταρα, δημιούργησε μια βιβλιοθήκη κλώνων που περιείχε 70 πληθυσμούς λανθάνοντα μολυσμένων μονοκυττάρων. Στη συνέχεια, η Blanco ανέλυσε τους κλωνικούς πληθυσμούς και τις αποκρίσεις τους στην ενεργοποίηση. Οι αποκρίσεις διέφεραν σημαντικά, υπογραμμίζοντας τη μεγάλη ποικιλομορφία σε έναν μεμονωμένο τύπο κυττάρου.
Αυτή η παρατήρηση εγείρει ένα νέο ερώτημα: Οι διαφορετικοί τύποι κυττάρων παρουσιάζουν πραγματικά διαφορετικές αποκρίσεις στις θεραπείες λανθάνουσας κατάστασης του HIV; Πράγματι, τα αποτελέσματα της μελέτης τους έδειξαν ότι ορισμένα αντι-HIV λανθάνοντα θεραπευτικά μπορούν να προάγουν τον λανθάνοντα χρόνο στα Τ κύτταρα και τα μονοκύτταρα, ενώ στα μακροφάγα μπορούν να αντιστρέψουν τον λανθάνοντα χρόνο.
"Δεν είναι όλα τα κύτταρα του σώματος ίδια", είπε ο Kieffer. "Έτσι είναι λογικό ότι δεν θα ανταποκριθούν όλα τα μολυσμένα κύτταρα στον ιό με τον ίδιο τρόπο."
Η εργασία τους υπογραμμίζει την ανάγκη για μελλοντικές θεραπείες για τον HIV να λαμβάνονται υπόψη όλοι οι τύποι κυττάρων και πώς κάθε κύτταρο μπορεί να ανταποκριθεί σε πιθανές θεραπείες.
Τα ευρήματά τους βασίζονται σε έρευνα του Roy Dar, πρώην καθηγητή βιομηχανικής του Ιλινόις, του οποίου το εργαστήριο μελέτησε την ετερογένεια στην έκφραση του γονιδίου HIV.
"Το ξεκίνησε και το αναλάβαμε και το φέραμε εκεί που είναι τώρα", είπε ο Kieffer. "Έτσι η συνεργασία ξεκίνησε πραγματικά αυτά τα αποτελέσματα. Έχει μετατραπεί σε μια νέα κατεύθυνση για το εργαστήριό μας και είμαστε πολύ ενθουσιασμένοι γι 'αυτό."
Ένα επιπλέον και απροσδόκητο εύρημα από την ανάλυση του Blanco αποκάλυψε αλλαγές στο μέγεθος και το σχήμα των κυττάρων ως απόκριση στη μόλυνση, υποδηλώνοντας ότι ο HIV μπορεί να αλλάξει τη μορφολογία των κυττάρων. Ο επόμενος στόχος του Blanco είναι να προσδιορίσει τους βιολογικούς μηχανισμούς που βρίσκονται πίσω από αυτές τις φαινοτυπικές αλλαγές.
Ο Kieffer και τα μέλη του εργαστηρίου του ανυπομονούν επίσης να αναπαράγουν τα αποτελέσματά τους, τα οποία έγιναν σε μεγάλο βαθμό σε μια κυτταρική γραμμή, σε πρωτεύοντα κύτταρα. Η αναπαραγωγή των αποτελεσμάτων σε ένα μοντέλο που μοιάζει περισσότερο με τον άνθρωπο θα βελτίωνε την κλινική συνάφεια της μελέτης, εξήγησε ο Kieffer.
"Θα θέλαμε να κάνουμε μεγαλύτερες οθόνες σε Τ κύτταρα, μονοκύτταρα και μακροφάγα για να εντοπίσουμε πιθανά φάρμακα που θα μπορούσαν να λειτουργήσουν σε όλους αυτούς τους κυτταρικούς τύπους", είπε ο Blanco. "Θα μπορούσαμε να βρούμε ακόμη περισσότερα μόρια που δεν συμπεριφέρονται με έναν συγκεκριμένο τύπο κυττάρου."
