Νέες δημοσιεύσεις
Το φάρμακο LM11A-31 επιβραδύνει την εξέλιξη της νόσου του Alzheimer σε δοκιμή
Τελευταία επισκόπηση: 02.07.2025

Όλα τα περιεχόμενα του iLive ελέγχονται ιατρικά ή ελέγχονται για να διασφαλιστεί η όσο το δυνατόν ακριβέστερη ακρίβεια.
Έχουμε αυστηρές κατευθυντήριες γραμμές προμήθειας και συνδέουμε μόνο με αξιόπιστους δικτυακούς τόπους πολυμέσων, ακαδημαϊκά ερευνητικά ιδρύματα και, όπου είναι δυνατόν, ιατρικά επισκοπικά μελέτες. Σημειώστε ότι οι αριθμοί στις παρενθέσεις ([1], [2], κλπ.) Είναι σύνδεσμοι με τις οποίες μπορείτε να κάνετε κλικ σε αυτές τις μελέτες.
Εάν πιστεύετε ότι κάποιο από το περιεχόμενό μας είναι ανακριβές, παρωχημένο ή αμφισβητήσιμο, παρακαλώ επιλέξτε το και πατήστε Ctrl + Enter.

Σε μια πρόσφατη μελέτη που δημοσιεύτηκε στο περιοδικό Nature Medicine, οι επιστήμονες διεξήγαγαν μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη φάσης 2α για να εξετάσουν την ασφάλεια και την αποτελεσματικότητα του LM11A-31 στη θεραπεία της νόσου Αλτσχάιμερ (AD) μέσω της τροποποίησης του υποδοχέα νευροτροφίνης p75 (p75NTR).
Η όψιμης έναρξης νόσος Alzheimer (AD) είναι η πιο κοινή μορφή άνοιας, που χαρακτηρίζεται από συναπτική ανεπάρκεια, εκφύλιση και απώλεια νευρικών κυττάρων. Αν και τα δύο κορυφαία φάρμακα για τη θεραπεία της AD στοχεύουν στη συσσώρευση μη φυσιολογικών πρωτεϊνών αμυλοειδούς-β ή tau, αντιμετωπίζουν μόνο ένα μέρος της παθοφυσιολογίας. Μια άλλη προσέγγιση περιλαμβάνει τη στόχευση υποδοχέων και δικτύων σηματοδότησης που επηρεάζουν θεμελιώδεις βιολογικές οδούς. Προκλινικές μελέτες δείχνουν ότι η τροποποίηση του p75NTR με ένα νέο μικρό χημικό μόριο, το LM11A-31, μειώνει την απώλεια συνάψεων που προκαλείται από την αμυλοειδή και την μη φυσιολογική tau πρωτεΐνη.
Περιγραφή της μελέτης
Σε αυτήν την τυχαιοποιημένη κλινική δοκιμή, οι ερευνητές εξέτασαν εάν το LM11A-31 θα μπορούσε να επιβραδύνει την εξέλιξη της νόσου Αλτσχάιμερ τροποποιώντας το p75NTR στους ανθρώπους.
Στους συμμετέχοντες στη μελέτη χορηγήθηκαν από του στόματος κάψουλες LM11A-31 σε δόσεις των 200 mg και 400 mg ή εικονικό φάρμακο σε αναλογία 1:1:1 σε 242 ασθενείς με ήπιο έως μέτριο άσθμα για 26 εβδομάδες. Οι συμμετέχοντες είχαν βιολογικά επιβεβαιωμένη νόσο Αλτσχάιμερ (επίπεδο πρωτεΐνης β42 αμυλοειδούς β στο εγκεφαλονωτιαίο υγρό κάτω από 550 ng/L ή αναλογία Aβ42:β40 κάτω από 0,89) διαγνωσμένη σύμφωνα με τα κριτήρια McKhann, με βαθμολογίες Mini-Psychiatric Examination (MMSE) από 18 έως 26, βαθμολογίες στην Κλίμακα Γηριατρικής Κατάθλιψης (GDS) κάτω από 5,0, βαθμολογίες στην Τροποποιημένη Κλίμακα Ισχαιμικής Κλίμακας Hachinski (HIS) ≤ 4,0, επίσημη εκπαίδευση ≥ 8 έτη και προηγούμενη γνωστική έκπτωση ≥ 6 μηνών.
Οι επιλέξιμοι συμμετέχοντες είχαν λάβει αναστολείς ακετυλοχολινεστεράσης (AChEIs) ή μερικούς ανταγωνιστές υποδοχέα NMDA για ≥ 3 μήνες πριν από την ένταξή τους στη μελέτη. Δεν έλαβαν παράνομες ουσίες όπως αντιψυχωσικά, βενζοδιαζεπίνες, αντιεπιληπτικά φάρμακα, ηρεμιστικά, κεντρικά δραστικά αντιυπερτασικά, νοοτροπικά (εκτός από ginkgo biloba) ή αναλγητικά που περιέχουν οπιοειδή.
Το κύριο αποτέλεσμα της μελέτης ήταν η ασφάλεια και η ανεκτικότητα, όπως αξιολογήθηκαν χρησιμοποιώντας την Κλίμακα Αξιολόγησης Σοβαρότητας Σκέψεων και Συμπεριφοράς Columbia (C-SSRS), τα ζωτικά σημεία, η αρτηριακή πίεση και οι αιματολογικές παράμετροι. Χρησιμοποιήθηκαν δομική μαγνητική τομογραφία (cMRI), τομογραφία εκπομπής ποζιτρονίων με φθοροδεοξυγλυκόζη (FDG-PET) και βιοδείκτες εγκεφαλονωτιαίου υγρού (CSF) για την αξιολόγηση δευτερογενών γνωστικών αποτελεσμάτων. Οι μετρήσεις της AD περιελάμβαναν Thr181-φωσφορυλιωμένη tau, ολική πρωτεΐνη tau, Aβ40, Aβ42 και δραστηριότητα AChE. Η ομάδα χρησιμοποίησε ένα προσαρμοσμένο νευροψυχολογικό τεστ για την αξιολόγηση δευτερογενών γνωστικών αποτελεσμάτων κατά την έναρξη, τις εβδομάδες 12 και 26.
Αποτελέσματα έρευνας
Η μελέτη διαπίστωσε ότι το LM11A-31 είναι ασφαλές και καλά ανεκτό, χωρίς σημαντικές ανησυχίες για την ασφάλεια. Οι πιο συχνές ανεπιθύμητες ενέργειες περιελάμβαναν πονοκέφαλο, διάρροια, ηωσινοφιλία και ρινοφαρυγγίτιδα, με τα γαστρεντερικά προβλήματα και την ηωσινοφιλία να είναι οι κύριοι λόγοι διακοπής. Υπήρξαν περισσότερες διακοπές στην ομάδα των 400 mg σε σύγκριση με τις ομάδες των 200 mg και του εικονικού φαρμάκου. Η μαγνητική τομογραφία δεν αποκάλυψε ανησυχίες για την ασφάλεια, συμπεριλαμβανομένων ανωμαλιών που σχετίζονται με το αμυλοειδές. Δεν υπήρχαν σημαντικές διαφορές στις γνωστικές βαθμολογίες ή στις ανωμαλίες του αμυλοειδούς μεταξύ των δύο ομάδων θεραπείας.
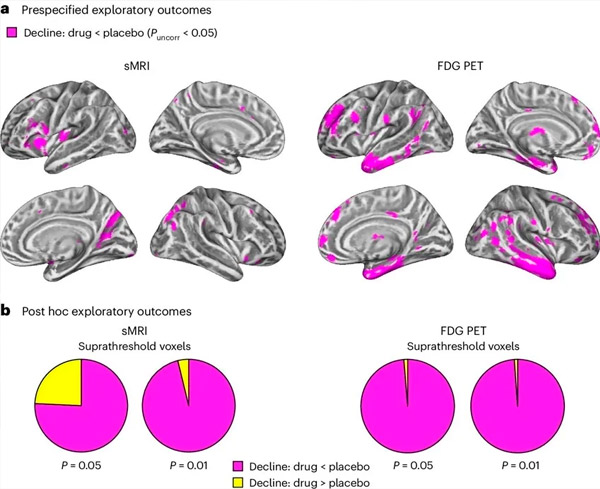
Α. Η αμφίδρομη ανάλυση μικτών μοντέλων συνδιακύμανσης εξέτασε τις αλληλεπιδράσεις μεταξύ της θεραπείας (φάρμακο ή εικονικό φάρμακο) και του χρόνου (πριν ή μετά τη θεραπεία). Μια μονόπλευρη t-αντίθεση που εξέτασε την υπόθεση αλληλεπίδρασης (το φάρμακο επιβραδύνει την εξέλιξη σε σύγκριση με το εικονικό φάρμακο) έδειξε ότι η θεραπεία με LM11A-31 επιβράδυνε τη διαμήκη εκφύλιση (αριστερά πλαίσια) και τον υπομεταβολισμό της γλυκόζης (δεξιά πλαίσια) στην ομάδα φαρμάκου (cMRI, n = 127· PET, n = 121) σε σύγκριση με την ομάδα εικονικού φαρμάκου (cMRI, n = 66· PET, n = 62). Τα Voxels που δείχνουν αυτήν την αλληλεπίδραση εμφανίζονται σε ένα μη διορθωμένο όριο P < 0,05 (ματζέντα) σε μια ειδική για τον πληθυσμό φλοιώδη επιφάνεια. Τα αριστερά και τα δεξιά ημισφαίρια εμφανίζονται στις επάνω και κάτω σειρές, αντίστοιχα. Οι περιοχές του εγκεφάλου που εμφανίζουν αλληλεπιδράσεις ασύμβατες με την υπόθεση φαίνονται στο Σχήμα 7 στα Συμπληρωματικά Δεδομένα.
Β. Συνολικός αριθμός voxels σε προκαθορισμένες ευάλωτες περιοχές του εγκεφάλου με νόσο Alzheimer (συνολική επιφάνεια κυκλικών διαγραμμάτων) που δείχνουν είτε μια αλληλεπίδραση σύμφωνα με την υπόθεση (ματζέντα) είτε μια αλληλεπίδραση ασύμβατη με την υπόθεση (κίτρινο) σε κάθε απεικονιστική μέθοδο (cMRI, αριστερό πλαίσιο· FDG PET, δεξί πλαίσιο) σε ολοένα και πιο ελεύθερα όρια μη διορθωμένου P < 0,01 και P < 0,05. Οι προσομοιώσεις Monte Carlo έδειξαν ότι οι αναλογίες των voxels που εμφάνιζαν επιδράσεις σύμφωνα με την υπόθεση έναντι ασύμβατων με την υπόθεση ήταν σημαντικά υψηλότερες από αυτές που παρατηρήθηκαν με βάση τυχαία παραγόμενα δεδομένα τόσο για cMRI όσο και για PET (P < 0,001 για κάθε μέθοδο· αμφίπλευρη δοκιμή).
Το LM11A-31 μείωσε αποτελεσματικά την αύξηση των επιπέδων Aβ42 και Aβ40 στο εγκεφαλονωτιαίο υγρό (ΕΝΥ) σε σύγκριση με την ομάδα του εικονικού φαρμάκου. Το φάρμακο έδειξε επίσης μείωση στη μέση ετήσια ποσοστιαία μεταβολή του προσυναπτικού πρωτεϊνικού βιοδείκτη SNAP25 και μείωση του μετασυναπτικού βιοδείκτη NG, υποδεικνύοντας επιβράδυνση της απώλειας προσυναπτικών και μετασυναπτικών συνδέσεων. Το LM11A-31 μείωσε επίσης την αύξηση του YKL40, οδηγώντας σε μείωση των βαθμολογιών MMSE και αύξηση των βαθμολογιών ADAS-Cog-13. Το φάρμακο μείωσε επίσης την απώλεια φαιάς ουσίας στον μετωπιαίο λοβό και τον οπίσθιο βρεγματικό φλοιό και μείωση του μεταβολισμού της γλυκόζης σε περιοχές όπως ο ενδορινικός φλοιός, ο κροταφικός φλοιός, ο ιππόκαμπος, ο νησιδικός φλοιός και ο προμετωπιαίος φλοιός.
Σύναψη
Η μελέτη κατέληξε στο συμπέρασμα ότι η τροποποίηση του p75NTR από το LM11A-31 είναι κατάλληλη για μεγαλύτερες κλινικές δοκιμές. Το LM11A-31 πέτυχε το κύριο καταληκτικό σημείο ασφάλειας και ήταν καλά ανεκτή σε ασθενείς με ήπια έως σοβαρή νόσο Alzheimer. Τα αποτελέσματα υποδεικνύουν την ανάγκη για περαιτέρω μελέτες με μεγαλύτερη διάρκεια θεραπείας για την αξιολόγηση της δυνατότητας μικρών μορίων να ρυθμίζουν το p75NTR ως θεραπεία τροποποίησης της νόσου στη νόσο Alzheimer. Η μελέτη έδειξε ότι το LM11A-31 επηρέασε σημαντικά αρκετούς βιοδείκτες, συμπεριλαμβανομένων των Aβ40, Aβ42, SNAP25, NG και YKL40, υποδεικνύοντας επιβράδυνση της παθολογικής εξέλιξης. Μελλοντικές μελέτες ενδέχεται να αξιολογήσουν πρόσθετους δείκτες της υγείας των νευρογλοιακών κυττάρων.
